2017年 筑波大学 大学院人間総合科学研究科 博士課程修了 博士(医学)
2018年 Albert Einstein College of Medicine, Research Fellow
2021年 群馬大学 生体調節研究所 博士研究員
2023年 新潟大学 医学部医学科研究推進センター 技術職員
2024年 徳島大学 先端酵素学研究所 助教


サイト内検索

2014年 東北大学 大学院生命科学研究科 博士課程修了 博士(生命科学)
2014年 日本学術振興会 特別研究員(SPD)
2017年 東京大学 分子細胞生物学研究所 助教
2018年 日本学術振興会 海外特別研究員
2018年 Albert Einstein College of Medicine, Research Fellow
2021年 科学技術振興機構(JST)さきがけ専任研究者
2023年 徳島大学 先端酵素学研究所 准教授
生命を支える遺伝子発現は、DNAがmRNAへと転写され、mRNAが蛋白質へと翻訳されることで実行されます。私たちの研究室では、細胞内1分子イメージング技術を駆使して、長年にわたる遺伝子発現の謎を解き明かすべく研究を行っています。
私たちは現在、遺伝子発現の後半部分にあたる翻訳をメインに研究を進めています。翻訳はあらゆる生命機能に必須の現象であり、例えば新型コロナウイルスのパンデミックで脚光を浴びたmRNAワクチンも翻訳されなければ機能することができません。その重要性ゆえに、これまで翻訳について世界中で研究が行われてきましたが、その大部分は実は生化学的な実験手法(細胞をすり潰した溶液を試験管の中で解析する手法など)によるものです。そのため、翻訳がどのように制御されているのかといったメカニズムについては理解が進んでいる一方、翻訳が細胞内において「いつ・どこで」制御されているのかといった時空間的な側面については驚くほど理解が遅れています。そこで私たちは、翻訳の制御過程を細胞内において実際に「見る」ことができる独自の新規イメージング技術を武器に、長年ベールに包まれてきた翻訳の時空間的な側面について解析を進めています。
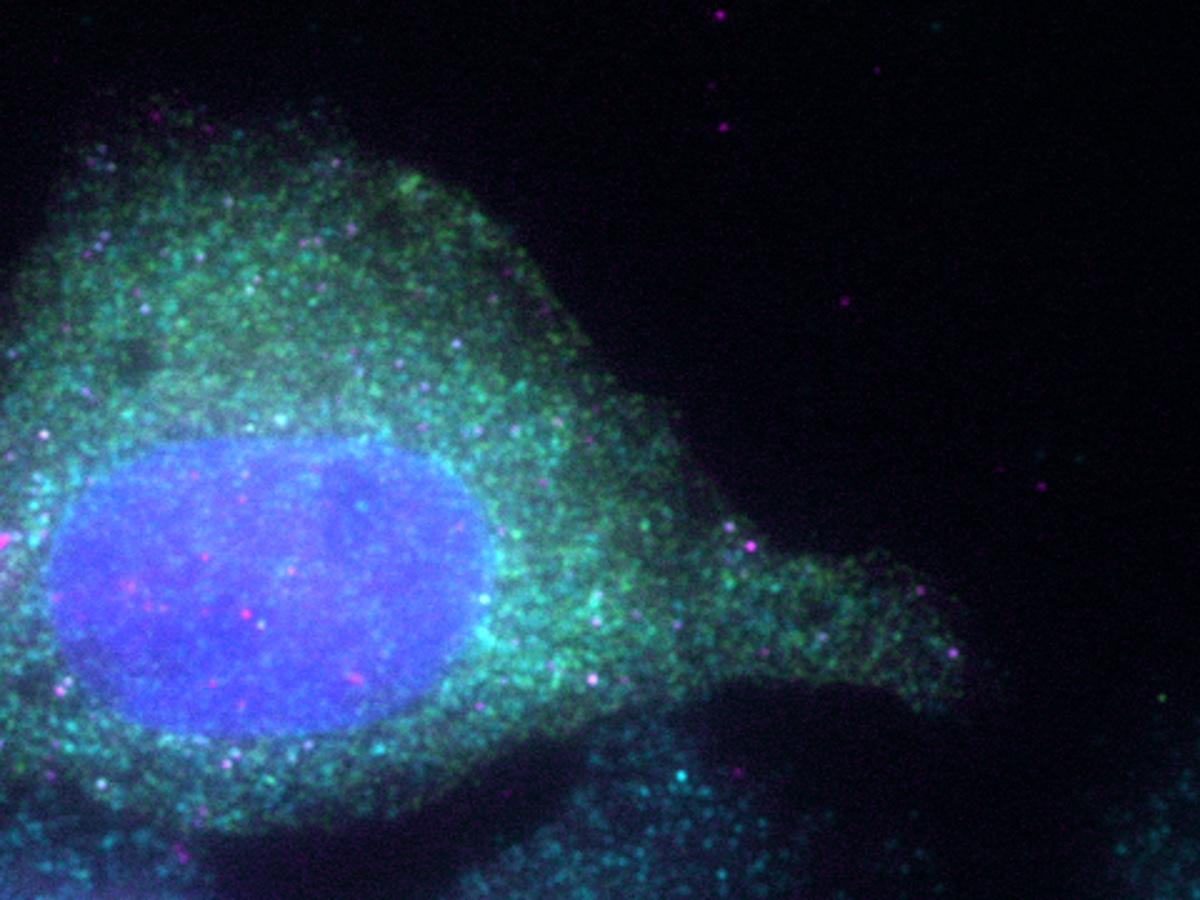
これまで翻訳の研究を支えてきた生化学的な実験手法では、数多くの細胞から回収された数多くのmRNAの「集団」について解析が行われてきました。そのため、細胞1つ1つ、mRNA 1つ1つがどういった翻訳の挙動を示すのかという点についても、長らく知るすべがありませんでした。従来の手法とは異なり、私たちが開発したイメージング技術では(図:Kobayashi & Singer, 2022, Nature Communicationsより一部改変)、翻訳制御を1細胞かつ1分子mRNA解像度で「見る」ことが可能です。そこで私たちは、この技術的なアドバンテージを活かし、知られざる翻訳の1細胞レベルの個性、1分子mRNAレベルの個性についても解析を進めています。
Copyright©2019 Institute of Advanced Medical Sciences, Tokushima University