分子細胞形態学分野

2009年 総合研究大学院大学 生命科学研究科 生理科学専攻 修了 博士(理学)
2009年 岡崎統合バイオサイエンスセンター ナノ形態生理研究室 特別研究員
2011年 Max Planck Institute of Biochemistry, Department of Molecular Structural Biology, PostDoc
2018年 東京大学大学院 医学系研究科 生体構造学分野 特任助教
2020年 東京大学大学院 医学系研究科 生体構造学分野 特任講師
2023年 徳島大学 先端酵素学研究所 准教授
研究概要
全ての生物において“ 細胞膜”は、細胞内外の隔離をはじめ、生命現象において様々な機能を担っています。したがって、生命現象のさらなる理解には、細胞における膜機能の解明が重要であると考えられます。当研究室では、クライオ電子線トモグラフィー(クライオET)およびクライオ集束イオンビーム (クライオFIB)を用いた構造解析を主な手法として、生体膜機能の解明を目指しています。
1.オートファジーにおける隔離膜膜動態の研究
オートファジーは、細胞内における不要な構造を分解することでタンパク質やオルガネラの品質管理などを担う、生命の維持に重要な現象であることが知られています。オートファジーでは、隔離膜という二重の脂質二重膜を持つ特徴的な膜構造が分解対象を包み込みながら伸長しオートファゴソームを形成します。そして、オートファゴソームがリソソームもしくは液胞と融合することで、対象物の分解を行います。オートファジーにおいて、隔離膜がどのように形成され、どのようにしてオートファゴソームへの構造の変化をもたらす分子基盤はいまだに不明です。本研究では、細胞内での隔離膜の形成過程を観察することで、隔離膜の形態変化を担う構造基盤および膜動態の作動原理を解明することを目指します。
2.古細菌における膜機能の研究
古細菌は地球上のいたるところに生息しており、高温、高pH、高塩濃度などの極限環境において生息している古細菌も存在します。一般的な古細菌は細胞壁を有していますが、特定の古細菌は細胞壁をもたないにもかかわらず過酷な環境に生息している種も存在します。私たちは高温、強酸性環境で生息しているが細胞壁をもたない古細菌に着目し、この古細菌の細胞膜がどのようにして極限環境に適応しているのかを解明することを目指します。
3.クライオFIB用凍結生物試料作製法の開発
クライオFIBを用いて凍結生物試料を微細加工することによって、核などの細胞内深部構造をクライオ電子線トモグラフィーで観察することが可能となりました。しかしながら、生物試料の導電性が悪いことから、作製したラメラの帯電による観察像の歪み等の問題があります。そのため、私たちは試料のクライオFIB用に試料の帯電を抑えた凍結生物試料作製法の開発を行うことで、クライオFIBとクライオETを組み合わせた構造解析法の高効率化を目指します。
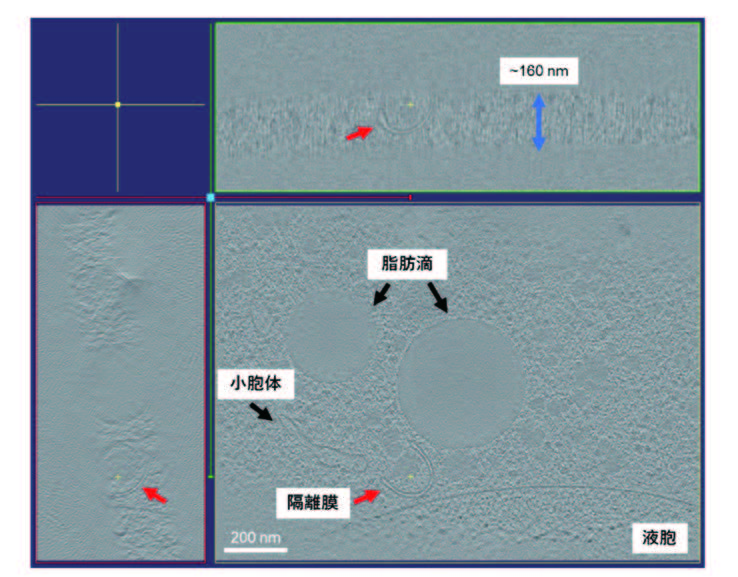
図1.酵母細胞内隔離膜のクライオ電子線トモグラフィー像
最近の主要論文
- Gipson P, Fukuda Y, Danev R, Lai Y, DH, Baumeister W, Brunger AT. Morphologies of synaptic protein membrane fusion interfaces. Proc. Natl. Acad. Sci. USA 114:9110-9115 (2017).
- Fukuda Y, Beck F, Plitzko JM, Baumeister W. In situ structural studies of tripeptidyl peptidase II (TPPII) reveal spatial association with proteasomes. Proc. Natl. Acad. Sci. USA 114:4412-4417 (2017).
- Fukuda Y, Laugks U, Lučić V, Baumeister W, Danev R. Electron cryotomography of vitrified cells with a V olta phase plate. J. Struct. Biol. 190:143-154 (2015)
- Asano S, Fukuda Y, Beck F, Aufderheide A, Förster F, Danev R, Baumeister W. A molecular census of 26S proteasomes in intact neurons. Science 347:439-442 (2015)








